

Anabolismo de Desoxiribonucleotídeos |
 |
|
|
|
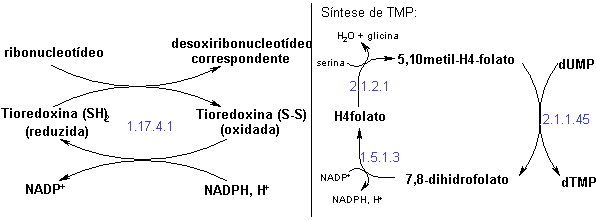
Tanto nos mamíferos como em microorganismos, são formados a partir de seus ribonucleotídeos correspondentes pela reposição do grupo 2’-OH por um hidrogênio (ou seja, do grupo 2’-oxi por 2’-desoxi). Os substratos para esta reação, catalisada pela ribonucleotídeo redutase, são ribonucleosídeos difosfato. O substrato redutor fisiológico é uma proteína de baixo peso molecular transportadora de elétrons, a tioredoxina. |
|
A ribonucleotídeo redutase é notável pelo fato de seu mecanismo de reação prover o exemplo melhor caracterizado do envolvimento de radicais livres nas transformações bioquímicas. Desta forma, ela é um protótipo para as reações envolvendo radicais intermediários, uma vez tidos como raros nos sistemas biológicos. |
|
Como o DNA possui timina (5-metil-uracil) em lugar da uracila dos ribonucleotídeos, o timidilato é sintetizado a partir de dUMP, e há muitas formas pelas quais este último pode ser sintetizado nas células. Um caminho possível, é a deaminação de dCMP, de acordo com a seguinte reação catalisada pela deoxicitidilato deaminase: |
|
dCMP
+ H2O |
|
Outra via que é provavelmente de grande importância, é a redução de UDP a dUDP, seguida da fosforilação deste a UTP, que por sua vez é hidrolisado a UMP. |
|
dUTP + H20
|
|
Timina é, similarmente
à Uracila, convertida a dTMP de acordo com as seguintes reações: |
|
Timina
+ deoxiribose-1-P
|
|
Timidina + ATP
|
|
A timidina fosforilase foi purificada tanto em bactérias como em tecidos de mamíferos. Timidina é o substrato preferido, mas deoxiuridina e seus derivados com substitutos na posição 5 também são clivados. A timidina quinase é amplamente distribuída. |