 |
 |
 |
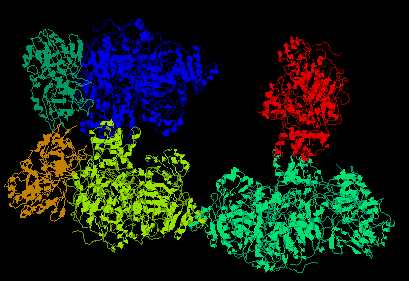
Clique sobre a figura para abrir/fazer o download do arquivo PDB (tridimensional e interativo)
Glutamina-dependente carbamoil-P sintase
GD-CPSase
Carbamil P sintetase (glutamina)
L-Glutamina
CO2
H2O
Orto-P
L-Glutamato
Carbamoil-P
Carbamoil-P sntase (CPSase) cataliza a síntese ATP-dependente de carbamoil-P a partir de glutamina no citosol (EC 6.3.5.5) ou amônia (EC 6.3.4.16) e bicarbonato na mitocôndria. CPSase inicia tanto o ciclo da uréia quanto a síntese de arginina e pirimidinas.
CPSase glutamina dependente (CPSase II) está envolvida na biossíntese de pirimidinas e purinas. Em bactérias como Escherichia coli, uma única enzima está envolvida em ambas as vias, enquanto em outras bactérias há enzimas separadas. Em bactérias é formada por duas subunidades. Uma cadeia pequena possui atividade glutamina amidotransferase (GATase) necessária à remoção do grupo amino da glutamina, e uma cadeia maior possui a atividade CPSase. Esta estrutura também está presente em fungos para a biossíntese de arginina. Na maioria dos eucariontes, os três primeiros passos da biossíntese de pirimidinas são catalizados por uma grande enzima multifuncional - chamada URA2 em leveduras, rudimentar em Drosophila e CAD em mamíferos. O domínio CPSase está localizado entre um domínio GATase N-terminal e a porção C-terminal, que detém as atividades dihidroorotaase e aspartato transacarbamilase.
A CPSase amônia-dependente (CPSase I) está envolvida no ciclo da uréia em vertebrados ureotélicos; é uma proteína monofuncional localizada na matriz mitocondrial.
O domínio CPSase é tipicamente de 120KDa, e surgiu da duplicação de um subdomínio ancestral de 500 resíduos de aminoácidos. Cada subdomínio liga-se independentemente a ATP e foi sugerido que cada uma das metades homólogas atua separadamente, um para catalisar a fosforilação de bicarbonato a crboxi-P e outro de carabamato a carbamil-P.
O subdomínio
CPSase também está presente como cópia única
nas enzimas biotina-dependentes acetil-CoA carboxilase
(EC 6.4.1.2) (ACC), propionil-CoA carboxilase
(EC 6.4.1.3) (PCCase), piruvato carboxilase
(EC 6.4.1.1) (PC) e uréia
carboxilase (EC
6.3.4.6). Como assinatura para o subdomínio foram seecionadas
duas regiões conservadas, provavelmente importantes na ligação
ao ATP e/ou atividade catalítica.
Referência